Estequiometria
Seleccione la respuesta correcta y justifica tu elección.
1. ¿Cuántas moléculas de anhídrido sulfúrico (SO3), Equivalen a la masa de 4 moles de calcio?
a.
8 moles.
- b. 6 moles.
- c. 0,5 moles.
- d. 2 moles
Justificacion___________________________________________________________________
2. ¿Cuántas moléculas de hay en 3 moles CO2 ?
- a. 3.
- b. 9.
- c. 9 x6, 02x1023
- d. 3x6, 02x1023
- e. 30x6, 02x1023
Justificacion___________________________________________________________________
3. La masa molar del sodio es 23 g/mol. Por lo tanto, 5 moles de este elemento corresponde a
a. (5/23)g- b. (23/5)g
- c. (23 +5)g
- d. (23 . 5)g
- e. 23g
Justificacion___________________________________________________________________
4. La formula química NO2 puede representar a
I) Una molécula de NO2
II) Un mol de NO2
III) 6, 02x1023 moléculas de NO2
- a. Solo la I
- b. Solo la II
- c. Solo la III
- d. I. II y III
- e. Solo II y III
Justificacion___________________________________________________________________
5. ¿Cuántos moles existen en 106g de K3 PO 4 (PM K3 PO 4 212 g/mol)?
a. 1,75 mol- b. 0,8 mol
- c. 1 mol
- d. 0.5 mol
- e. 2 mol
Justificacion___________________________________________________________________
6. 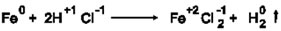
De acuerdo con la ecuación planteada si se cambia el hierro Fe por dos moles de sodio Na0 probablemente se formara
- a. 2NaCl + H2
- b. NaCl + H2
- c. 2NaH + Cl2
- d. NaCl2 + H2
Justificacion___________________________________________________________________
CONTESTE LAS PREGUNTAS 7 Y 8 DE ACUERDO CON LA SIGUIENTE ECUACIÒN
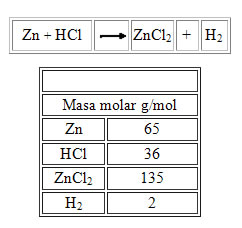
7. Es válido afirmar que la ecuación anterior, cumple con la ley de la conservación de la materia, porque:
- a. el número de átomos de cada tipo en los átomos productos es mayor que el número de de cada tipo en los reactivos
- b. la masa de los productos es mayor que la masa de los reactivos
- c. el número de átomos de cada tipo en los reactivos es igual al número de átomos del mismo tipo en los productos
- d. el número de sustancias reaccionantes es igual al número de sustancias obtenidas
Justificacion___________________________________________________________________
8. De acuerdo con la ecuación anterior, es correcto afirmar que:
- a. 2 moles de HCl producen 2 moles de ZnCl2 y 2 moles de H2
- b. 1mol de Zn produce 2 moles de ZnCl2 y 1 mol de H2
- c. 72 g de HCl producen 135 g de ZnCl2 y 1 mol de H2
- d. 135 g de ZnCl2 reaccionan con 1 molécula de H2
|